1. 全国9批中药材及中药饮片检出金胺O
23日,国家食品药品监督管理总局在其官网发布通告称,近期,食品药品监管总局在全国范围内组织对黄柏、延胡索等中药材及中药饮片进行了专项监督抽验,分别从药品生产、经营和使用环节进行了抽样,检出9批不合格。
通告中指出,经重庆市食品药品检验检测研究院检验,发现标示为安国市万联中药饮片有限公司、安徽易元堂中药饮片科技有限公司、安徽沪昆中药饮片有限公司、亳州市长生中药饮片有限公司、亳州市贡药饮片厂、国药控股广西中药饮片有限公司6家药品生产企业生产的7批黄柏检出金胺O;经广州市药品检验所检验,发现标示为安国市辉发中药饮片加工有限公司生产的1批延胡索、运城市风陵渡开发区华昌药业有限公司售出的1批延胡索检出金胺O。
金胺O是化学染色剂,曾发现被用于劣质黄柏、蒲黄、延胡索等中药材、中药饮片的非法染色。金胺O对人体具有一定毒性作用,被列为非食用物质,在中药材、中药饮片和中成药中均不得检出。对上述不合格药品,相关企业和单位所在地省(区)食品药品监管部门已依法采取了查封扣押、暂停生产、要求企业召回产品等控制措施。
根据通告,标示为安徽沪昆中药饮片有限公司生产的批号为130801的黄柏系从太原市长寿堂药店有限公司小店部抽取的样品,标示为亳州市贡药饮片厂生产的批号为141215的黄柏系从福建鸿越医药有限公司抽取的样品,两家生产企业均否认产品为本企业生产。
通告中提出,请山西、福建省食品药品监管局彻底查清不合格产品来源,请安徽省食品药品监管局对上述两家企业生产销售情况进行调查核实。请山西省食品药品监管局彻查运城市风陵渡开发区华昌药业有限公司不合格延胡索的产品来源。调查处理情况于2015年11月15日前报告食品药品监管总局,并及时向社会公布。
通过此次事件,反映出尽管当前国家对中药材源头和流通的监管更加严厉,但在中药材市场中依然存在一些违法行为。“整治”的不彻底,并不能一味的把责任全追究于国家监管部门,我们每一位消费者更应该积极主动的参与到监督检举的队伍中来。充分行使好公民具有的权利和义务。这样,才能确保我们的健康和利益不受侵害。
来源:中药材天地网; 链接:
http://www.zyctd.com/article-224503-1.html
2. 医药流通企业现状与发展思考
当前,医药工业的发展趋势是“换挡、变速、趋缓”;药品招标在各省市实施原则使药品降价已成常态;药品使用终端由于“二个总量控制”与“药占比的规定”导致同比增速下降;尤其是“互联网+”的新模式在处方一旦放开后的发展态势及快递业强势介入配送等原因,将导致整个产业链中的流通环节生存环境严峻与商业模式出现颠覆性的变化。 我国经济发展方式正从规模速度型粗放增长转向质量效率型集约增长,经济结构正从增量扩能为主转向调整存量、做优增量并存的深度调整,经济发展动力正从传统增长点转向新的增长点。
目前医药产业集中度提高与行业“多、小、散”产业格局并存。行业在通过一段时间的并购、重组过程之后,一定程度上提高了产业集中度,尤其是药品流通企业,前100位的药品批发企业已占到64.28%的市场份额。从批发企业数量分析:2014年的法人批发企业数量与2012年相比,减少比率为28.63%,短短的三年的时间,超四分之一的药品批发企业消失了。

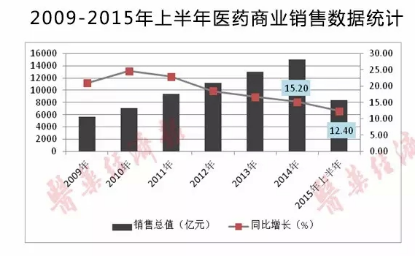
2015年上半年,虽大型药品流通企业的主营业务收入、利润增长、费用控制普遍优于行业整体水平,对行业发展的引领作用进一步提升,但药品流通行业总体销售增长放缓、运营成本增加、毛利率降低等一系列现实情况,对全行业发展形成了较大压力。
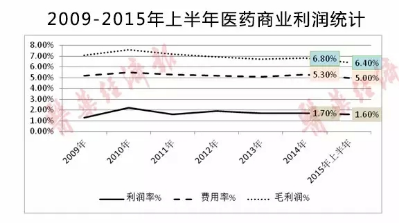
上市公司共17家,市值总值为2593亿元,平均市值为152.54亿元。规模过百亿的企业有15家,其中在800亿元以上的有3家。
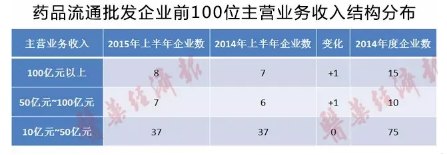
2015年上半年,医药电子商务继续快速发展。据国家食品药品监督管理总局统计,2015年上半年共批准、换发证书105家,截至2015年6月30日,拥有互联网交易资质的企业合计为425家,企业数量同比增长56.3%,其中B2B为90家、B2C为319家、O2O为16家,主要的交易模式为B2B、B2C形式,其中B2B占销售额比重为90%(O2O模式不含其中)。
我国现有的医药产品的分销模式越来越受到挑战,比如,传统终端采购时间需要与商业工作时间的冲突矛盾;推广手段与渠道单一及信息传达不足产生的矛盾;市场维护与开发成本高之矛盾;人员成本越来越高与吸引高端人才能力差所发生的矛盾。
终端的物流成本、回款周期与客户信用不足等问题也是商业无法回避的问题;还有互联网对传统医药流通渠道的影响,互联网的发展解决了一个最大的问题就是“信息不对称”,这对传统医药流通影响非常大,而且也将是趋势。
未来剩下的医药流通可能会因为以下的价值而存在:终端配送职能,尤其是医疗机构,毕竟专业产品需要专业的通道。
人口迁移因素,国内城镇化率在2014年已达到54.77%,未来可引导1亿多农民就近城镇化落户,带来新的健康医疗需求;老龄社会激活银发市场,利好健康产业的发展;新增出生人口持续增加,促使医疗保健需求市场旺盛。 国家持续不断地释放医疗服务资源、零售药店持续不断地发展完善、医药电子商务迅速地兴起,均为药品流通行业提供了拓展市场的机会和动力。
互联网技术将持续冲击并深刻改变行业面貌。药品流通行业供应服务保障体系如何适应未来的公共卫生、计划生育、医疗服务、医疗保障、健康管理等系统,如何实现业务协同与支撑,并且构建连通各级平台和各医疗卫生机构的供应信息网络。
实行并优化医药供应链,使企业尽快转型为医药供应链服务提供商。当前企业主要战略整合商机在于品类采购和医药物流的整合,使传统分销模式转型升级为创造价值链的营销模式。所有企业应在转型创新中快速整合和优化医药供应链,并与战略合作伙伴及利益相关方做到无缝对接。
充分利用互联网技术,搭建医药电子商务平台,扩展新的消费市场。如针对慢病患者设计坚持用药与用药常识咨询服务的模块;采用电子健康管理咨询服务方式,设计患者和医疗专业人员进行实时互联互通的服务模块;学会使用医药电子商务扩大营销市场、扩大对医疗机构的服务渠道及扩大社区药店对慢病患者终端覆盖的服务商机。
树立服务大健康理念,驱动健康消费。围绕大健康产业和消费形态,拓展创新服务产品及服务模式。开展对健康人群的服务,并通过建立“互联网+”的协作,与信息技术相结合创造健康组合服务产品,扩展新的消费市场。
不断推进国际合作,创新医药供应链服务模式。有条件的企业可以与国际大健康业态有关的资本技术密集型服务企业合作,引进先进的健康管理技术与服务产品,大胆探索引进国际医药物流、国际金融结算、分销零售业务等功能。
国家对长江经济带、京津冀一体化、“一带一路”等重大战略的提出,将进一步带动国内经济发展,并提供巨大的投资发展机遇。对于医药行业来说,尤其要注意长三角地区的医药产业技术升级、河北医药行业对京津产业转移的承接、中医药服务贸易及相关产业对西部地区经济发展的拉动等正面因素,使企业发展战略融入国家大战略之中,不断拓展新的终端医疗消费市场和健康服务市场。
来源:医药经济报; 链接:
http://www.catcm.org.cn/newsmain.asp?id=7342&tid=&cname=
1. 浅谈质检改革发展的原则与路径
质检改革要遵循以下几个原则:
一是依法依规原则。要以法治的思维和创新的思维,妥善解决改革创新与依法行政的冲突。一方面要建立健全质检法律法规,避免出现法律的盲区和监管漏洞;另一方面对特定改革区域和领域进行法律授权,允许突破现有法律法规的改革试点。
二是党的领导原则。质检改革已进入深水区,必须要有刮骨疗伤的勇气和魄力,否则很难打破自身利益和部门利益的藩篱。
三是顶层设计原则。基层的改革创新虽然非常重要,但是必须首先得到上级的授权或认可,否则就会违反“法无授权不可为”的原则。因此质检改革主要应该从国家层面、质检总局层面自上而下进行。
在遵循以上原则的基础上,质检改革可按如下路径逐步展开:
第一,打造进出口产品质量安全的“宏观监测”机制。转变工作思路,从以微观质量检验为主转向以宏观质量监测为主;从防范具体产品质量安全风险为主转向防范区域性、系统性产品质量安全风险为主;从以执法把关为主转向执法与服务并重。大力加强基于大数据和云计算的进出口产品、食品和进出境人员以及动植物质量安全信息的宏观监测能力建设,通过风险分析、风险评估和风险识别,实现精准执法和对重大质量安全风险的定点处置。大力加强有关国内外技术性贸易措施的跟踪、研究和评议队伍建设,建立技术性贸易措施通报、咨询、评议、预警综合信息系统,为国内企业“走出去”战略提供技术和信息支撑。
第二,构建检管分离的质检工作体制。出口工业产品取消法定检验以来,一方面大量政府检验检测资源闲置浪费无法全力参与市场竞争,另一方面外资合资检验检测资源又大举进入我国市场。根据国际惯例和市场化的发展趋势,检管分离是质检事业健康发展的必由之路。建议将中国检科院和各直属检验检疫局下辖的技术中心整合重组,组建另一个全国性的国有大型检验检测集团公司,该公司按市场化运作的同时,承担国家基准实验室职能。
第三、建立有利于人流物流“快进快出”的口岸执法体系。一是以电子口岸建设为基础,建立统一的口岸联检执法平台。该执法平台应由国家和地方口岸管理部门联合口岸联检单位共同建设,平等使用。二是在口岸联检单位建设方面,近期按照“信息互换、执法互助、监管互认”的原则,组建联合执法队伍,形成“一次申报、一次查验、一次放行”的快速通关工作模式。远期可参照“联合作战司令部”的战区模式,依托口岸联检单位现有资源,组建统一的口岸执法部门,形成海关、检验检验、边检、海事等诸兵种既专业分工又联合作战的新型口岸执法体系。三是按照“区港一体化”的工作思路,将口岸查验工作前推后移,充分发挥属地和特殊监管区检验检疫部门的工作潜力。只要是风险可控的进出口产品,原则上均须在辖区完成检验检疫,检验检疫结果全国通用,真正实现全国“通检通放”。
来源:凡特网; 链接:
http://www.vantlab.com/html/A7848801a9d0f4f5fa31ba78af4aa9095.html
2. 中药现代化可否走青蒿素之路?
中国女药学家屠呦呦因发现抗疟药物青蒿素,拯救无数生命,与另外两位科学家分享2015年诺贝尔生理学或医学奖,引发社会各界关注。
2011年获得美国拉斯克医学奖时,屠呦呦的获奖感言是,“这是中医中药走向世界的一项荣誉”。此次获得诺贝尔奖,屠呦呦说:“青蒿素是传统中医药送给世界人民的礼物。青蒿素的发现是集体发掘中药的成功范例。”
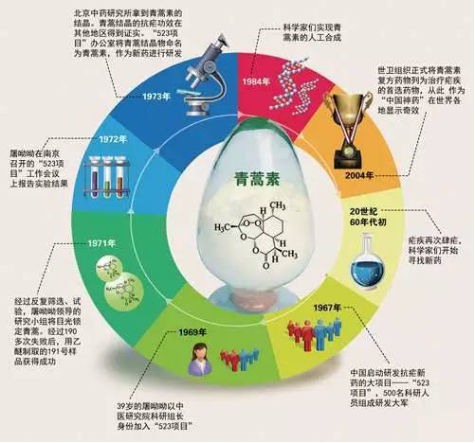
中国药科大学副校长、教育部长江学者特聘教授孔令义认为,青蒿素是天然药物,来源于中草药,而后来广泛应用的抗疟效果更好的青蒿素衍生物,则是结构修饰的产物,是化学药物即西药。其实,将化学药物和中药对立起来没有意义。复旦大学药学院教授陈道峰也认为,青蒿素的发现,其实是中药材的科学化研究,或者说是植物药的科学化研究,这是中药现代化的道路之一。
近年来,中药引起西方一些国家的重视,以植物药为例,西方有40家植物研究机构,500多个研究项目。在日本,许多汉方药企建立的研究机构从事汉方药物研究,建立了药材生产基地。美国NIH和艾滋病防治中心分别对300多种中草药进行筛选和有效成分研究,从植物药中寻找抗癌活性成本。
而国家食药监总局药品审评中心发布的《2014年度药品审评报告》显示,2014年149个获批上市的新药中,中药有11个,占比只有7.38%。
来源:中国中药协会; 链接:
http://www.catcm.org.cn/newsmain.asp?id=7313&tid=&cname=
1. 中药饮片标准规范长路漫漫
目前,中药饮片主要执行国家标准与地方标准。全国生产的中药饮片已经超过2000种,而现行的2010版《中国药典》共收载的中药饮片质量标准仅800多种,其他品种的生产只能执行省、自治区、直辖市人民政府药品监督管理部门制定的炮制规范。甚至有的饮片生产企业加工的饮片在国家标准和省级地方标准中都没有收载,也就是说根本没有检验依据,质量无法把控。
硫磺熏蒸是传统的中药材保存技法,目的是为防虫、防霉和杀菌。但中药材经过熏硫之后,不仅颜色好看还可增加重量。有媒体报道,50公斤百合熏硫后可以增加到60公斤。而国家规定,每公斤百合熏硫的硫磺含量不能超过150毫克。显然有许多企业达不到要求。事实上,一些中药材经过熏蒸后,硫磺含量超过国家规定几百倍。
长期以来,我国中药饮片执行的《中国药典》、《全国中药饮片炮制规范》、《各省市中药饮片炮制规范》三级标准,但标准之间并不完全统一,国家标准与地方标准之间、地方标准与地方标准之间在基源、名称(俗名、地方习惯用名的存在使得同名异物现象很多)、炮制规格及炮制方法等方面差别甚大,相同药材经常出现多种炮制方法,在生产、经营、使用、检验上没有明确规定,操作性不强。
有媒体报道,根据《药品生产质量管理规范2010年版》认证要求,中药饮片生产企业要在2015年12月31日前,必须通过国家新版GMP认证,否则不得继续生产。根据国家食品药品监督管理总局的统计数据,截至2013年12月,我国取得中药饮片GMP资格认证的企业有1580家。而由于质量问题频发,不少企业被收回了GMP证书。
中药材种植规范化难度很大,小作坊式种植生产、同一药材多地收购的现象普遍存在,每个品种短时间内无法达成规范化规模化种植,质量差异大。中药饮片的基源复杂,中药材同品种多产地的情况普遍,导致中药材的显微特征、性状、药性有差异。中药材、中药饮片的质量均匀性差,不同产地、不同来源质量差异较大。因此要完全弄清各种药材或中药饮片的成分和疗效,制订统一的中药饮片质量标准不是一朝一夕的事情。
基于中药饮片这一类药品的特殊性,针对目前全国中药饮片质量标准存在的部分品种质量标准科学适用性不强,中药饮片质量标准不完善,许多常规习用品种无标准可执行等问题,国家药监部门可建立省级中药饮片企业标准备案机制。
在进行充分的试验研究和数据收集的基础上,企业可针对市场需求大但无标准可执行或国家标准制订不合理的中药饮片,制订中药饮片企业标准,向所在地的省级药监部门进行中药饮片企业标准备案,一并提供研究资料来佐证企业标准制订的合理性和科学性;省级药监部门在受理后进行形式审查、专家评审和核查,对符合要求的企业标准准予备案并下发备案的中药饮片企业标准,并进行公示。
同时,实行国家标准与注册标准相结合的办法,建议药监部门制订中药饮片注册制度和相关指导原则,保障该注册标准的落地实行。协会可以组织制定相关标准在协会内部推荐实行,企业也可根据自身的实际情况以及研究的数据,制定出高于国家标准的“内控标准”来进行注册申请。这样可以促进中药饮片质量标准的完善和提高,企业注册标准的申请和执行也对国家标准的完善具有很好的指导作用。
针对不同中药饮片的质量标准或标准的各项具体质量指标,采取渐进的方式,成熟一项,制定一项,执行一项。从而使得我国中药饮片加工企业、医疗机构、零售药店等能够按规范统一的标准实施,从而确保中药饮片质量合格有效,发挥出中药应有的治疗效果。
来源:中药材天地网; 链接:
http://www.zyctd.com/article-224669-1.html